Caso clínico: Paciente con marcapasos DDDRO en seguimiento remoto con sistema Latitude™
Por María José Sancho-Tello de Carranza, Pedro Pimenta Fermisson-Ramos, Óscar Cano Pérez, Joaquín Osca Asensi, Ana Andrés Lahuerta, Pau Alonso Fernández y José Olagüe de Ros.
Unidad de Arritmias, Hospital Universitario y Politécnico La Fe, Valencia.
Autor de correspondencia: María-José Sancho-Tello de Carranza
Correo electrónico: mjstdc@gmail.com
Introducción
El seguimiento remoto de dispositivos de estimulación cardiaca (DEC) fue introducido en la práctica clínica en el año 2000 por BIOTRONIK. Desde entonces hasta ahora, todas las empresas fabricantes de DEC han desarrollado sus sistemas de monitorización y seguimiento remoto aplicables en su mayoría a marcapasos (MP) y desfibriladores automáticos implantables (DAI). Básicamente todos los sistemas consisten en un receptor-transmisor que recoge la información almacenada en el DEC y la envía de forma encriptada, a través de la línea de telefonía fija o móvil a un servidor seguro, donde se desencripta y se almacena en una página web que es revisada por los profesionales sanitarios de forma segura mediante identificación con nombre de usuario y contraseña. Los datos obtenidos son superponibles a los que se obtienen en una interrogación con el programador durante las visitas presenciales. Los seguimientos remotos pueden programarse con una periodicidad preestablecida y también desencadenarse por alertas clínicas o de funcionamiento del DEC que son programables en la mayoría de los casos. Así mismo el propio paciente puede iniciar una transmisión no programada ante la presencia de síntomas o a requerimiento de los profesionales sanitarios.
Existe evidencia científica acumulada de que el seguimiento remoto es fiable y seguro (1,2), reduce visitas presenciales, permite la detección precoz de eventos asintomáticos (3,4), predice descompensaciones e ingresos por insuficiencia cardiaca (IC) (5-6), acorta estancias hospitalarias (4), mejora la eficiencia de la utilización de recursos sanitarios y la calidad de la asistencia (7) y disminuye el número de descargas inapropiadas en DAI (8), así como la mortalidad (9). Así mismo es bien aceptado por los pacientes (10). Es de resaltar el importante papel del seguimiento remoto en la detección y manejo de la fibrilación auricular asintomática (11-13), que es frecuente tanto en pacientes con MP, en los que además es predictor independiente de mortalidad cardiovascular (14), como en pacientes con IC (15), los que a su vez también reúnen otros factores de riesgo tromboembólico. Así también, la monitorización remota ayudaría al manejo de la anticoagulación en estos pacientes, pudiendo contribuir a una reducción en la presentación de ictus (13,16).
Caso Clínico
Presentamos el caso de una paciente con marcapasos bicameral en seguimiento remoto con sistema de monitorización remota de Boston Scientific.
Se trata de una paciente de 80 años, con antecedentes de HTA, DM tipo 2, dislipemia y cardiopatía reumática a la que se le implantaron 2 prótesis valvulares mecánicas en posición aórtica y mitral en 1990. La paciente ha seguido controles periódicos en la consulta de cardiología manteniendo buen estadio funcional para la disnea y con prótesis ambas normofuncionantes en ecocardiogramas seriados, buena función sistólica de VI y dilatación auricular izquierda (32,6 cm2 en plano apical de 4 cavidades), insuficiencia tricúspide moderada funcional y PSAP 60 mmHg). En su evolución presentó 2 episodios de fibrilación auricular persistente con deterioro de su estadio funcional, que precisó cardioversión eléctrica sincronizada y tratamiento antiarrítmico en 2009 y 2012 para mantenimiento de ritmo sinusal.
En tratamiento habitual con: Losartán, Digoxina, Bisoprolol, Sintrom, Furosemida, Espironolactona, Atorvastatina y Amlodipino.
En uno de los controles en consultas, la paciente refiere haber presentado 2 episodios de pérdida de conciencia, en reposo, con sensación de visión borrosa, no precedidos de mareo ni palpitaciones ni dolor torácico y con recuperación completa inmediata. Así mismo refiere episodios ocasionales de palpitaciones recortados.
Se realiza ECG de Holter de 24 horas que muestra una bradicardia sinusal persistente con frecuencia mínima de 33 lpm y máxima de 76 lpm, con frecuencia media de 46 lpm, sin pausas patológicas y con extrasistolia auricular escasa, con dobletes y salvas de hasta 9 latidos, con un tiempo de recuperación del seno tras taquicardia auricular de 1577 ms. Conducción aurículoventricular e intraventricular normales.
Con el diagnóstico de síncope de perfil cardiogénico y bradicardia persistente, aún con medicación bradicardizante, que es necesaria (antecedentes de fa) se indica la implantación de un MP bicameral con algoritmo de mínima estimulación en ventrículo derecho. (Indicación I nivel de evidencia B de las guías europeas de estimulación y resincronización cardiaca) (17).
Se implanta un MP doble cámara de Boston Scientific con sonda-electrodo auricular implantada en septo interauricular y sonda-electrodo ventricular implantada en septo interventricular bajo.
Estos son los parámetros eléctricos de implante:
UEstA = 0.8V @ 0,50 ms; EGMa = 2.1mV; ImpA = 593ohms
UEstVD = 0.3V @ 0,50 ms; EGMvd = 14.6mV; ImpVD = 657ohms
Se le proporciona seguimiento remoto con sistema de monitorización remota y se programa seguimiento remoto cada 6 meses y el sistema de alertas que viene reflejado en la figura 1. Tras realizar una primera visita presencial a los 3 meses del implante para programar el dispositivo se le informa a la paciente de que va a seguir el resto de controles de su MP de forma remota y será avisada si se detecta algún problema que así lo requiera. En ausencia de problemas se le enviarán informes con periodicidad anual.
En estos 2 años se han realizado 4 seguimientos remotos todos ellos programados, sin que haya sido necesario concertar visitas presenciales. La figura 2 muestra el informe del último de ellos correspondiente al 10/07/2014.
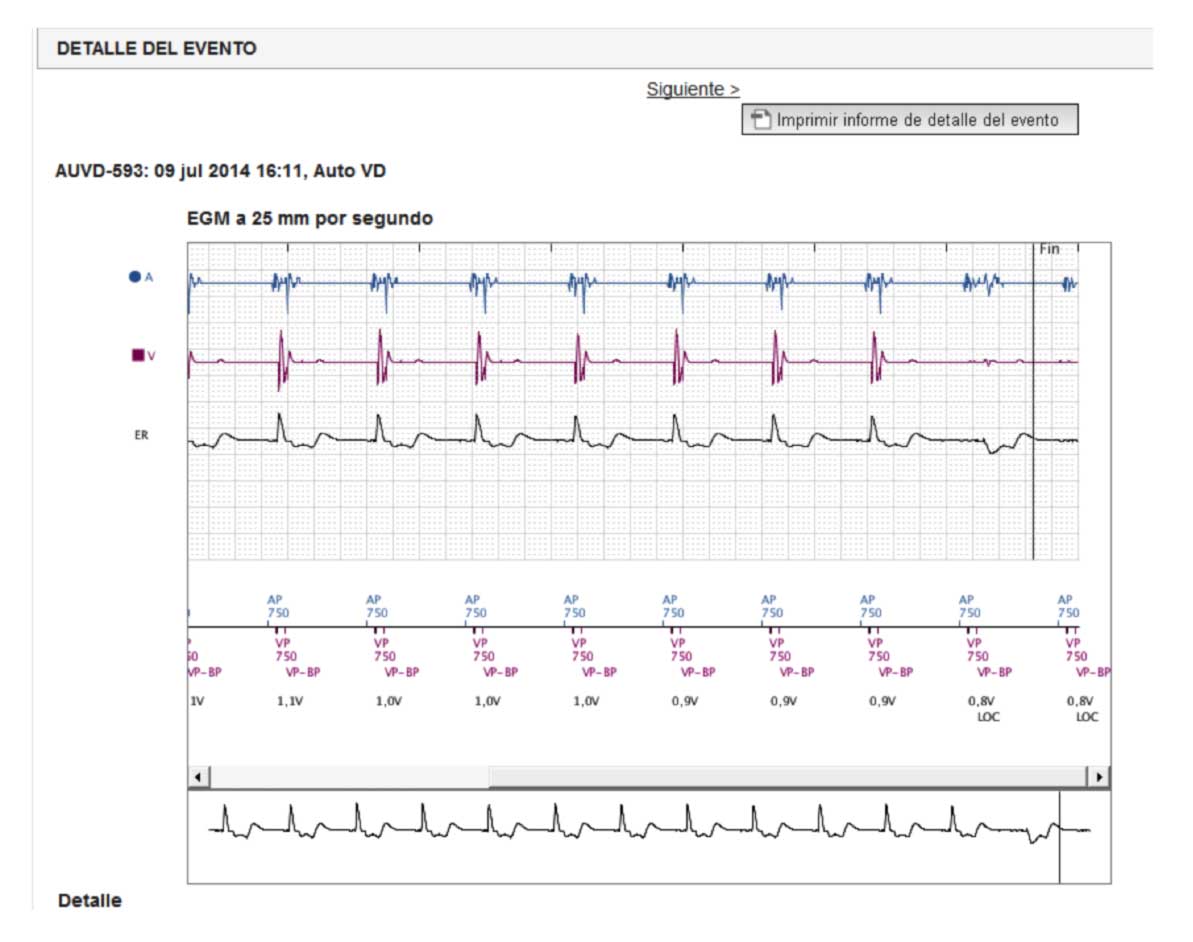
La figura 3 nos muestra la determinación automática del umbral de estimulación ventricular que es de 0,9 V@0,4 ms.
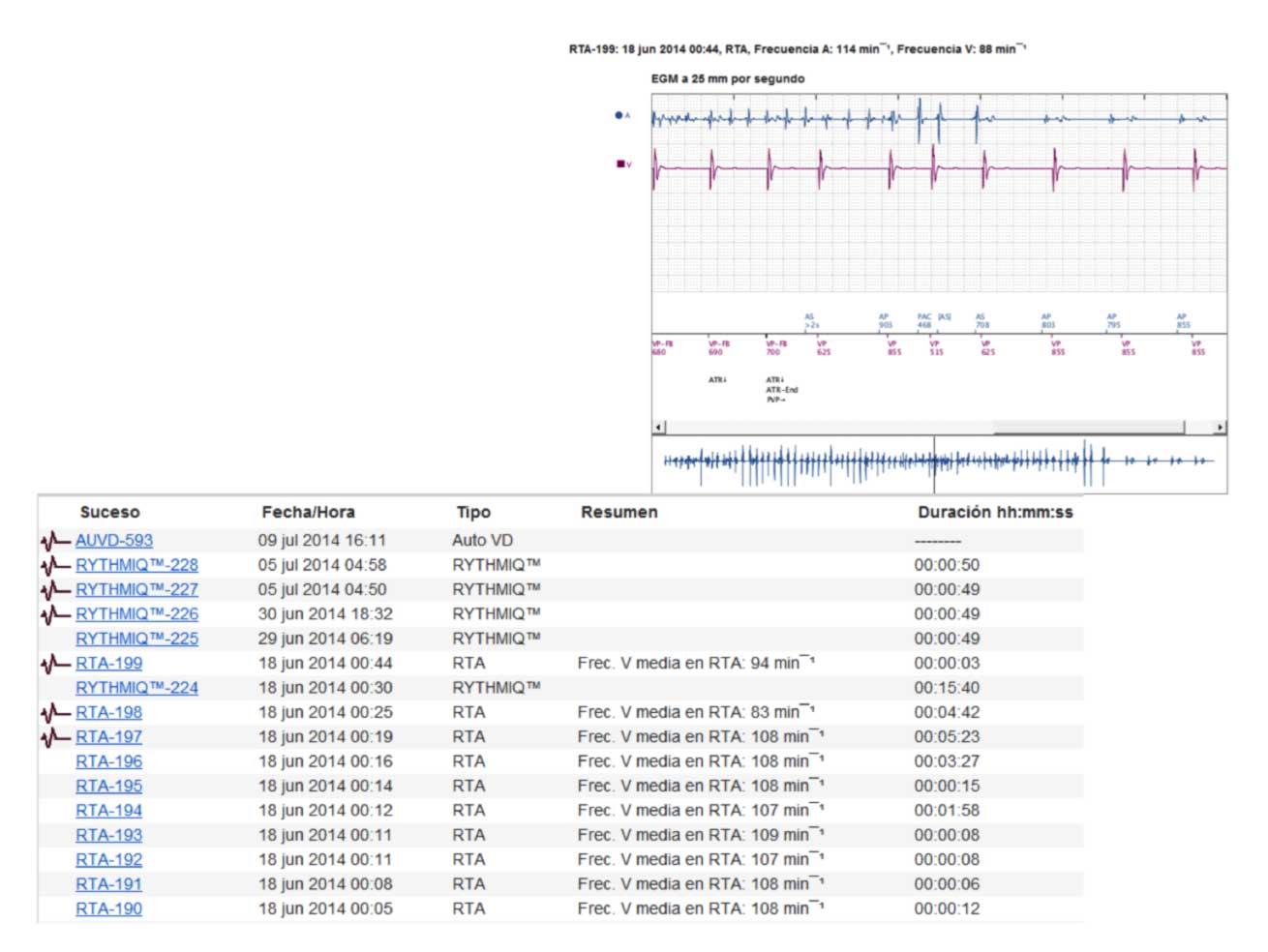
Figura 4: Registro de sucesos, que muestra episodios recortados de fibrilación auricular con respuesta ventricular controlada.
La figura 4 nos muestra el registro de sucesos con episodios autolimitados de fibrilación auricular, pero con respuesta ventricular controlada.
Discusión
El presente caso ilustra la posibilidad de seguimiento remoto de MP como sustitución de las visitas presenciales, a excepción de la primera tras el implante. Aun cuando las recomendaciones de expertos aconsejan una visita presencial de seguimiento del dispositivo al menos anual en pacientes con MP (18), sabemos que la necesidad de programación disminuye notablemente tras la primera visita y a lo largo de los años de duración de la batería (19). La información obtenida es superponible a la que se obtiene durante la visita presencial, por lo que es posible reducir las visitas presenciales únicamente a aquéllas en que sea necesaria la programación del dispositivo o la exploración física del paciente. Existe ya experiencia en nuestro país en este sentido (20)
En pacientes añosos, como son la inmensa mayoría de los pacientes con MP, que deben acudir frecuentemente al médico por sus distintas patologías, habitualmente acompañados por un familiar y en múltiples ocasiones con ambulancia, la sustitución de visitas presenciales por seguimiento remoto es de gran utilidad, aportando comodidad para el paciente y familiar, así como ahorro económico ya demostrado en pacientes con DAI (21-23) y también en pacientes ancianos y debilitados con MP (24).
Como ya hemos comentado en la introducción, la detección de arritmias auriculares asintomáticas es frecuente en paciente con MP (25). En esta paciente el seguimiento remoto no debería modificar el manejo de la anticoagulación, que viene marcado por el perfil de riesgo tromboembólico (26), que es elevado al ser portadora de prótesis valvulares, pero si nos permite un adecuado control clínico al poder evaluar duración y respuesta ventricular, con posibilidad de modificación de tratamiento farmacológico si fuera necesario para evitar descompensación clínica.
Aunque la implantación de unidades de seguimiento remoto de MP es aún escasa en nuestro país y en Europa (27), por diferentes motivos, la introducción de sistemas que permiten con un solo interrogador-transmisor el seguimiento de múltiples modelos de MP fabricados en los últimos años podrían extender y ampliar su utilización al poder realizar los seguimientos desde los centros de atención primaria e incluso desde residencias de ancianos.
Este caso refleja la opinión personal del individuo que lo ha realizado. Los casos clínicos no son necesariamente una predicción o representativos de las expectativas clínicas o de los resultados. El resultado real puede diferir en cada caso.
El contenido de este artículo es responsabilidad únicamente del autor y no representa la opinión de Boston Scientific.
Bibliografía:
1.- Lazarus A. Lazarus A. Remote, wireless, ambulatory monitoring of implantable pacemakers, cardioverter defibrillators, and cardiac resynchronization therapy systems: Analysis of a worldwide database. PACE 2007; 30:S2–S12.
2.- Osca J, Sancho-Tello MJ, Navarro J, Cano O, Raso R, Castro JE et al. Fiabilidad técnica y seguridad clínica de un sistema de monitorización remota de dispositivos cardiacos antiarrítmicos. Rev Esp Cardiol 2009; 62:886-95.
3.- Varma N, Michalsji J, Epstein AE, Schweikert R. Automatic remote monitoring of ICD lead and generador performance: the TRUST trial. Cir Arrhythm Electrophysiol 2010; 3:428-36.
4.- Crossley J, Boyle A, Vitense H, Chang Y, Mead H for the CONNECT investigators. The CONNECT (Clinical Evaluation of Remote Notification to reduce Time to Clinical Decision) trial. J Am Coll Cardiol 2011,57:1181-89.
5.- Whellan DJ, Ousdigian KT, Al-Khatib SM, Pu W, Sarkar S et al; PARTNERS study. Combined heart failure device diagnostics identify patients at higher risk of subsequent heart failure hospitalizations: results from PARTNERS HF study. J Am Coll Cardiol 2010; 55:1803-10.
6.- Sack S, Wende CM, Nägele H, Katzs A, Bauer WR, Barr CS et al. Potential value of automated daily screening of cardiac resynchronization therapy defibrillator diagnostics for prediction of major cardiovascular events: results from Home_CARE (Home Monitoring in Cardiac Resynchronization Therapy) study. Eur J Heart Fail 2011; 13:1019-27.
7.- Landolina M, Perego G, Lunati M, Curnis A, Guenzati G, Vicentini A et al. Remote monitoring reduces healthcare use and improves quality of care innheart failure patients with implantable defibrillators (EVOLVO) study. Circulation. 2012; 125;2985-92.
8.- Guedon-Moreau L, Lacroix D, Sadoul N, Clementy J, Kouakam C, Hermida JS et al.A randomized study of remote follow-up of implantable cardioverter defibrillators: safety and efficacy report of the ECOST trial. Eur Heart J 2013; 34:605–14.
9.- Saxon L, Hayes D, Roosevelt G, Heidenreich P, Day J, Seth M et al. Long term outcome after ICD and CRT implantation and influence of remote device follow-up. The ALTITUD survival study. Circulation 2010; 122:2359-67.
10.- Ricci RP, Moricelli L, Quarta L, Sassi A, Porfilli A, Laudadio MT et al. Long term patient acceptance and satisfaction with implanted device remote monitoring. Europace 2010;12:674-9.
11.- Ricci RP, Morichelli L, Santini M.Remote control of implanted devices through Home Monitoring technology improves detection and clinical management of atrial fibrillation. Europace 2009; 11:54–61.
12.- Ricci RP, Morichelli L, D’Onofrio A, Calo` L, Vaccari D, Zanotto Get al. Effectiveness of remote monitoring of cardiac implantable electronic devices in detection and treatment of clinical and device-related cardiovascular events in daily practice.: The HomeGuide Registry. Europace 2013; doi: 10.1093/europace/eus440. [Epub ahead of print].
13.- Mabo P, Victor F, Bazin P, Ahres S, Babuty D, Da Costa A et al. A randomized trial of long-term remote monitoring of pacemaker recipients (The COMPAS trial). Eur Heart J 2012; 33:1105–11.
14.- Gonzalez M, Keating R, Markowitz S, Liu Ch, Thomas G, Ip J et al. Newly detected atrial high rate episodes predict long-term mortality outcomes in patients with permanent pacemakers. Herat Rhythm 2014; 11:2214-21.
15.- Shanmugam N, Boerdlein A, Proff J, Ong P, Valencia O, Maier SK et al. Detection of atrial high-rate events by continuous home monitoring: clinical significance in the heart failure-cardiac resynchronization therapy population. Europace 14:230–7.
16.- Ricci R, Morichelli L, Gargaro A, Laudadio MT, Santini M. Home Monitoring in Patients with Implantable Cardiac Devices: Is There a Potential Reduction of Stroke Risk? Results from a Computer Model Tested ThroughnMonte Carlo Simulations. J Cardiovasc Electrophysiol 2009; 20:1244-51.
17.- Brignole M, Auricchio A, Barón-Esquivias G, Bordachar P, Boriani G, Breithardt OA et al. 2013 ESC Guidelines on cardiac pacing and cardiac resynchronization therapy: The Task Force on cardiac pacing and resynchronization therapy of the European Society of Cardiology (ESC). Developed in collaboration with the European Heart Rhythm Association (EHRA). Eur Heart J. 2013; 34:2281-329.
18.- Tracy C, Epstein A, Darbaar D, Di Marco J, Dunbar S, Estes M et al. 2012 ACCF/AHA/HRS Focused Update Incorporated Into the ACCF/AHA/HRS 2008 Guidelines for Device-Based Therapy of Cardiac Rhythm Abnormalities. J Am Col Cardiol 2013;61:e6-75.
19.- Van Eck JW, Van Hemel NM, de Voogt WG, Meeder JG, Spierenburgs HA, Crommentuyn H et al on behalf of the FOLLOWPACE investigators. Routine follow-up after pacemaker implantation:frequency, pacemaker programming and professionals in charge. Europace 2008;10:832-7.
20.- Al-Razzo =, González E, Sivestre J, Cabestrero D, Represa T, Alejandre M et al. Seguimiento domiciliario como sustitutivo de seguimiento presencial en pacientes portadores de marcapasos. Cuadernos de estimulación cardiaca 2011;4:57-62.
21.- Fauchier L, Sadoul N, Kouakam C, Briand F, Chauvin M, Babuty D et al. Potential cost savings by telemedicine-assisted long term care of implantable cardioverter defibrillator recipients. PACE 2005; 28:255S-59.
22.- Raatikainen MJ, Uusimaa P, Van Ginneken MM, Janssen JP, Linnaluoto M, Remote monitoring of implantable cardioverter defibrillator patients: a safe, time-saving, and cost-effective means for follow-up. Europace 2008;10:1145-51.
23.- Heidbuchel H, Hindricks G, Broadhurst P, Van Erven L, Fernandez-Lozano I, Rivero-Ayerza M et al. EuroEco (European Health Economic Trial on Home Monitoring in ICD Patients): a provider perspective in five European countries on costs and net financial impact of follow-up with or without remote monitoring. Eur Heart J. 2014 Sep 1. pii: ehu339. [Epub ahead of print]
24.- Folino A, Breda R, Calzavara P, Borghetti F, Comisso J, lliceto S et al. Remote follow-up of pacemakers in a selected population of debilitated elderly patients. Europace 2013;15:382-7.
25.- Healey JS, Connolly SJ, Gold MR, Israel CW, Van Gelder IC, Capucci A et al. ASSERT Investigators. Subclinical atrial fibrillation and the risk of stroke. N Engl J Med. 2012;366:120–129.
26.- Zimetbaum P, Waks JW, Ellis ER, Glotze TVr, Passman KS. Role of Atrial Fibrillation Burden in Assessing Thromboembolic Risk. Circ Arrhythm Electrophysiol. 2014;7:1223-1229.
27.- Hernández-Madrid A, Lewalter T, Proclemer A, Pison L, Lip G, Blomstrom-Lundqvist C et al. Remote monitoring of cardiac implantable electronic devices in Europe: results of the European Heart Rhythm Association survey.