Caso clínico: Estimulación ventricular parahisiana derecha
Por Alfonso Macías, Inés Madrazo, Miguel Angel Gómez-Sánchez
Unidad de arritmias y estimulación cardíaca. Hospital General Nuestra Señora del Prado. Talavera de la Reina. Toledo
La estimulación ventricular derecha, desde sus inicios, se ha realizado desde el ápex de ventrículo derecho (VD) fundamentalmente por tres razones: empleo de electrodos de fijación pasiva, técnica quirúrgica desarrollada y sencilla y buena estabilidad del electrodo1. Sin embargo, esta posición apical produce una comprobada asincronía en la activación del ventrículo izquierdo (VI). Esta asincronía da lugar a defectos de perfusión segmentarios, remodelado ventricular e incluso disfunción ventricular a largo plazo2. Además, se ha demostrado en diversos estudios, que un elevado porcentaje de estimulación apical se asocia a mayor incidencia de insuficiencia cardíaca y disminución de la fracción de eyección del VI (FEVI) 3.
Por tanto, es evidente que debemos evitar o minimizar en lo posible la estimulación desde ápex de VD, sobre todo en pacientes con historia de insuficiencia cardíaca y/o disfunción ventricular. Por otro lado, se han testado zonas ventriculares alternativas como el tracto de salida, la región septal y el haz de His. Si dichas zonas alternativas aportan mayores beneficios (o suponen menos perjuicios), es objeto aún de controversia y ha dado lugar a multitud de publicaciones 4,5.
La estimulación desde el tracto de salida de VD ha demostrado ser igualmente eficaz a la estimulación apical en términos de estabilidad a largo plazo de los parámetros eléctricos y sencillez técnica. Sin embargo, en los estudios comparativos entre ambas posiciones no se han obtenido resultados claramente superiores en variables como desarrollo de insuficiencia cardíaca o caída de fracción de eyección6,7. Similares datos se han obtenido con la estimulación medioseptal, disminuyendo la asincronía de VI pero sin aumento significativo de la fracción de eyección8, respecto a la estimulación apical.
Mejores resultados se han obtenido estimulando directamente el haz de His o la región parahisiana, que captura también miocardio adyacente. Al respecto, se han publicado estudios que reportan menos insuficiencia mitral e ingresos por insuficiencia cardiaca, además de un umbral mayor de estimulación ventricular en esta posición9.
Debido a la inconsistencia de los beneficios aportados por la estimulación de zonas alternativas respecto a la apical, las guías europeas de estimulación cardíaca no dan ninguna recomendación específica al respecto, si bien recomiendan minimizar la estimulación ventricular derecha siempre que sea posible10.
CASO CLÍNICO
Presentamos el caso de un varón de 51 años de edad, enviado a la consulta de arritmias en marzo de 2014 por intolerancia al ejercicio y bradicardia. Nunca había presentado síncopes.
Como factores de riesgo presentaba hipercolesterolemia con niveles de LDL alrededor de 130 mg/dl y en tratamiento con simvastatina 20 mg diarios.
No tenía antecedentes familiares de cardiopatía, muerte súbita ni portadores de marcapasos.
El ECG realizado en la consulta (Figura 1) mostraba un bloqueo AV completo con respuesta ventricular a 30 lpm, con QRS estrecho. En la historia clínica se encontró un ECG de hacía 5 años (preoperatorio de hallux valgus) con ritmo sinusal y bloqueo AV de primer grado (PR de 275 ms).
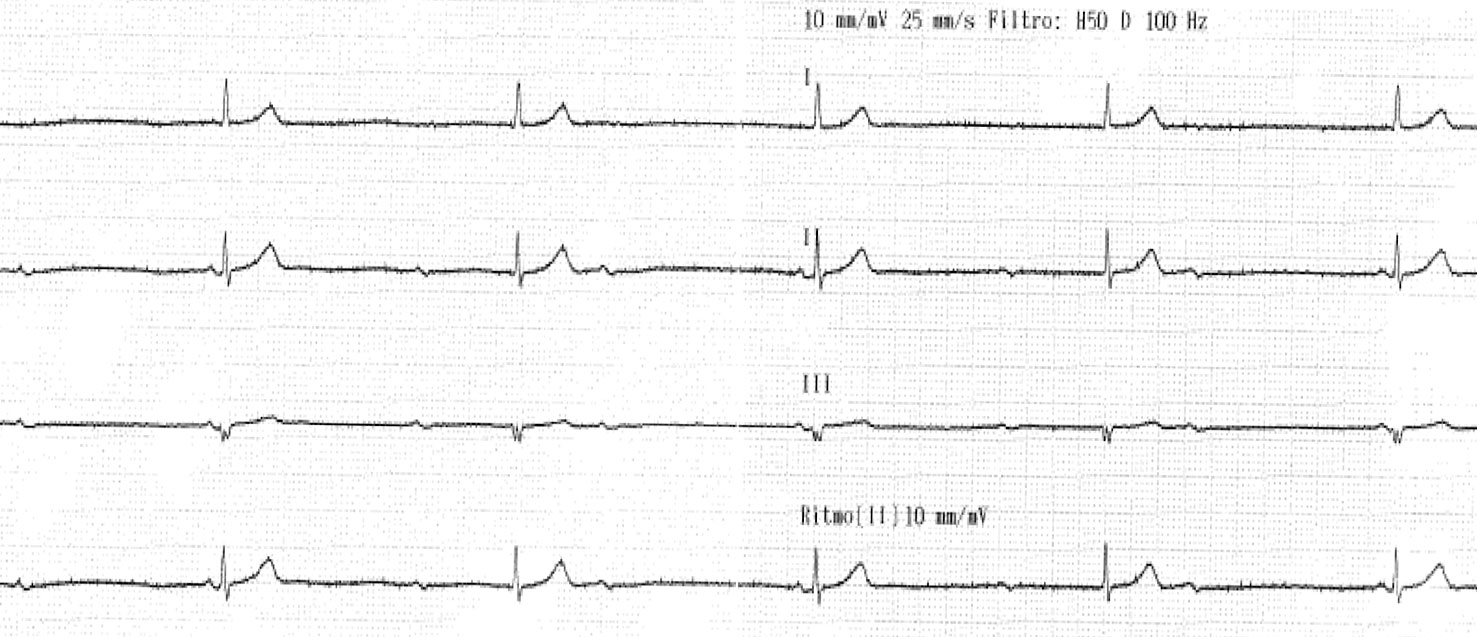
FIGURA 1: Tira de ritmo que muestra bloqueo AV completo
Se indicó ingreso para estudio cardiológico completo, realizándose las siguientes pruebas diagnósticas:
-Ecocardiograma: FEVI del 46%, con diámetro telediastólico de ventrículo izquierdo (DTDVI) de 58 mm, insuficiencia mitral grado I, dilatación biauricular. Ventrículo derecho con disfunción ligera.
-Resonancia magnética cardíaca: VI ligeramente dilatado (DTD 59 mm y VTD 203 ml) con función sistólica levemente disminuida (FEVI 48%). No alteraciones segmentarias de la contractilidad. GC de 4,1 l/min. VD ligeramente dilatado (VTD 204 ml) y función sistólica 45%. Dilatación biauricular (aurícula izquierda de 34 cm2 y aurícula derecha de 33 cm2). No hay captación patológica de contraste en las secuencias de realce tardío.
Ante estos hallazgos se propuso el implante de marcapasos, discutiéndose en sesión clínica el tipo de estimulación; convencional en ápex, sitios alternativos o biventricular. Finalmente se decidió intentar una estimulación parahisiana debido a la disfunción ventricular ligera, a un porcentaje de estimulación esperable del 100% y a un tiempo prolongado de estimulación dada la edad del paciente.
Se realizó de la siguiente manera:
1.- Disección de vena cefálica izquierda para el electrodo ventricular y punción de vena axilar izquierda para el electrodo auricular.
2.- Se emplearon dos electrodos de fijación activa de 52 y 59 cm de longitud, así como un generador DDDR de longevidad extendida. El sistema era compatible con resonancia magnética “full body”.
3.- Con el electrodo ventricular conectado a un polígrafo digital se mapeó la señal de His distal. Una vez registrada se progresó ligeramente el electrodo en sentido caudal, intentando anclarlo en una región parahisiana para capturar completamente el miocardio. Se realizaron las mediciones habituales: impedancia 1050 ohmios, onda R de 6 milivoltios y un umbral estable de 1,3 V a 0,5 ms. Posteriormente se implantó el electrodo auricular en la orejuela derecha. En la figura 2 se muestra la imagen final por radioscopia.
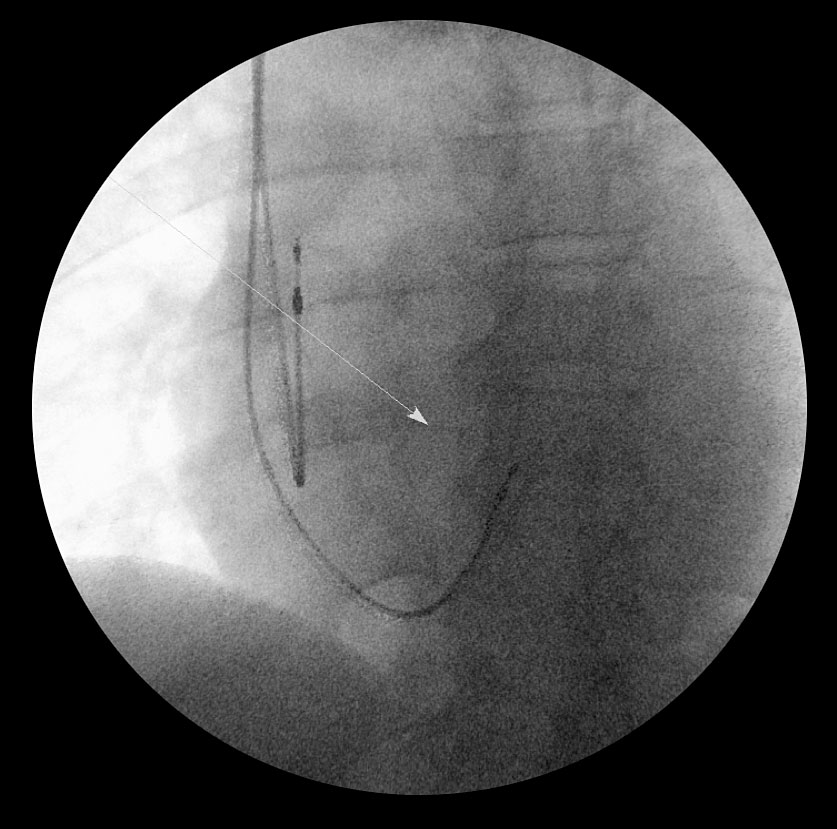
FIGURA 2A: Proyección posteroanterior (PA)
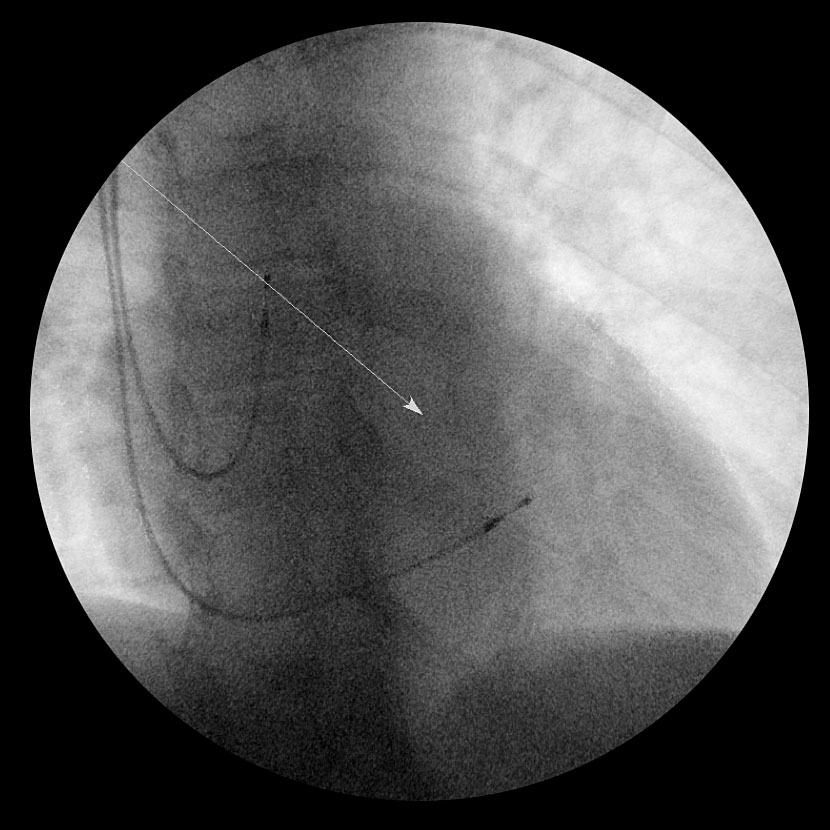
FIGURA 2B: Proyección oblicua anterior derecha (OAD) a 30º de la posición final de los electrodos.
4. El tiempo total de procedimiento (piel-piel) fue de 92 minutos y el tiempo de escopia de 13 minutos y 54 segundos (33.6 mGy).
A las 24 horas del implante se comprobó el buen estado de la herida quirúrgica, la ausencia de complicaciones en la Rx de tórax (figura 3) y la normofunción del dispositivo, por lo que fue dado de alta a su domicilio. En la figura 4 se muestra el ECG en el momento del alta.

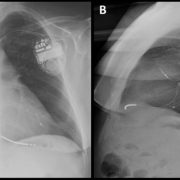
FIGURA 3: Rx de tórax a las 24 horas del procedimiento.
Posteriormente, el paciente fue visto en consulta de dispositivos al mes del implante y anualmente según nuestro protocolo habitual. Se encontraba asintomático cardiovascular, realizando vida activa. Los parámetros del generador se mostraban estables, con unas impedancias ventriculares de 950 ohmios y un umbral ventricular estable de 1,2 V a 0,4 ms.

FIGURA 4: ECG de 12 derivaciones post-implante.
En el último seguimiento, a los dos años del implante, se realizó un ecocardiograma que mostró un remodelado inverso con normalización de la FEVI (DTD 49 mm y fracción de eyección del 58% respectivamente). Las aurículas también habían disminuido de tamaño, presentando actualmente unos volúmenes prácticamente normales.
Aunque la mejora en estos parámetros ecocardiográficos probablemente sea debido a la corrección del efecto deletéreo del bloqueo completo, el modo de estimulación elegido, de momento, no ha sido perjudicial para nuestro paciente tras 2 años de seguimiento.
DISCUSIÓN
El presenta caso muestra una problemática no infrecuente que se nos plantea a la hora de elegir el modo y tipo de estimulación. Es un paciente de edad media, con disfunción VI ligera y alto porcentaje y tiempo de estimulación esperado.
Las guías actuales de dispositivos (10), en este caso, recomiendan una estimulación bicameral convencional sin recomendaciones sobre el lugar en el cual implantar el electrodo de VD. Por otro lado, las recientes guías de insuficiencia cardíaca11 recomiendan (clase I) la terapia de resincronización cardíaca (TRC) en pacientes con FEVI inferior o igual a 40% y alto porcentaje de estimulación esperado, existiendo datos inconsistentes en pacientes con FEVI normal.
En el caso actual, descartada la TRC, muy recomendable en este paciente en lugares con experiencia, se decidió que el ápex no era el lugar idóneo por las esperables consecuencias deletéreas anteriormente descritas. De las alternativas en el VD nos decantamos por la estimulación parahisiana por ser la estimulación con “más fisiológica”12 frente al tracto de salida y el septo. El tiempo de implante y escopia fueron más elevados que en un implante convencional pero la posición del electrodo era estable con umbrales aceptables para la estimulación crónica.
A este respecto se ha publicado un metaanálisis13 que mostró dos conclusiones principales: no existió diferencia a los 12 meses con respecto a la FEVI entre posiciones apicales y no apicales y la segunda, en pacientes con disfunción ventricular (inferior a 40%), la estimulación no apical era superior a la apical en términos de menor deterioro de la fracción de eyección. Sin embargo, en estos pacientes con disfunción ventricular ya ha sido publicado el claro beneficio de la TRC11. Apoyando al metaanálisis, el estudio Protect-Pace14 randomizó a 240 pacientes con FEVI normal (media de 57%) a recibir estimulación apical frente a estimulación septal alta con una estimulación ventricular esperada mayor del 90% por presentar los pacientes bloqueo AV de alto grado. La estimulación media fue del 99% y el seguimiento del estudio de 2 años. Al final del seguimiento la FEVI cayó en ambos grupos de forma ligera, pero sin diferencia alguna entre ambos grupos de estimulación. Tampoco se encontraron diferencias entre la tasa de ingresos por insuficiencia cardíaca, los niveles de péptido natriurético cerebral, la carga de fibrilación auricular ni en la mortalidad. Los autores concluyen que la estimulación septal no aporta beneficios con respecto a la estimulación apical tradicional en pacientes con función sistólica normal y estimulación ventricular del 100%.
CONCLUSIONES
La estimulación parahisiana puede ser de utilidad clínica en pacientes con disfunción ventricular izquierda ligera (FEVI 41-50%) y alto porcentaje de estimulación esperado, como alternativa a la estimulación apical.
Los resultados de los casos de estudio no son necesariamente predictivos de los resultados en otros casos. Los resultados de otros casos pueden variar. El contenido de este caso es responsabilidad únicamente del autor y no representa la opinión de Boston Scientific.
Bibliografía
1-. Kirkfeldt RE, Johansen JB, Nohr EA, Moller M, Arnsbo P, Nielsen JC. Risk facotrs for lead complications in cardiac pacing. Heart Rhythm 2011; 8 (10):1622-8.
2-. O`Keefe JH, Abuissa H, Jones PG, Thompson RC, Bateman TM, McGhie AI et al. Effect of chronic right ventricular apical pacing on left ventricular function. Am J Cardiol 2005; 95 (6):771-3.
3-. Thambo JB, Bordachar P, Garrigue S, Laffite S, Sanders P, Reuter S, et al. Detrimental ventricular remodeling in patients with congenital complete heart block and chronic right ventricular apical pacing. Circulation 2004; 110 (25): 3766-72.
4-. Gong X, Su Y, Pan W, Cui J, Liu S, Shu X. Is right ventricular outflow tract pacing superior to right ventricular apex pacing in patients with normal cardiac function?. Clinical Cardiology 2009; 32 (12): 695-9.
5-. Victor F, Mabo P, Mansour H, Pavin D, Kabalu G, De Place C, et al. A randomized comparison of permanent septal versus apical right ventricular pacing: short term results. Journal Cardiovasc Electrophysiol 2006; 17 (3): 238-42.
6-. Leong DP, Mitchell AM, Salna I, Brooks AG, Sharma G, Lim HS, et al. Long-term mechanical consequences of permanent right ventricular pacing: effect of pacing site. Journal Cardiovasc Electrophysiol 2010; 21 (10): 1120-6.
7-. Wang F, Shi H, Sun Y, Wang J, Yan Q, Jin W, et al. Right ventricular outflow pacing induces less regional wall motion abnormalities in the left ventricle compared with apical pacing Europace 2012; 14 (3): 351-7.
8-. Cano O, Osca J, Sancho-Tello MJ, Sanchez JM, Ortiz V, Castro JE, et al. Comparison of effectiveness of right ventricular septal pacing versus right ventricular apical pacing. Am J Cardiol 2010; 105 (10): 1426-32.
9-. Barba R, Moriña P, Venegas J, Frutos M, Moreno V, Herrera M. Posibilidades y realidades de la estimulación permanente del haz de His. Rev Esp Cardiol 2008; 61: 1096-9.
10-. Bignole M, Auricchio A, Baron G, Bordachar P, Boriani G, Breithardt OA, et al. 2013 ESC Guidelines on cardiac pacing and cardiac resynchronization therapy . Eur Heart J 2013; 34 (29): 2281-329.
11-. 2016 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure. Eur Heart J 2016; online version.
12-. Sharma PS, Dandamudi G, Naperkowski A, Oren JW, Storm RH, Ellenbogen KA, et al. Permanent His Bundle Pacing is Feasible, Safe and Superior to right ventricular pacing in routine clinical practice. Heart Rhythm 2014.
13-. Shimony A, Eisenberg MJ, Filion HB, Amit G. Beneficial effects of right ventricular non-apical vs apical pacing: a systematic review and meta-analysis of randomized-controlled trials. Europace 2012; 14 (1): 81-91.
14-. Kaye GC, Linker NJ, Marwick TH, Pollock L, Graham L, Pouliot E, et al. Effect of right ventricular pacing lead site on left ventricular function in patients with high grade atrioventricular block: results of the Protect-Pace study. Eur Heart J 2015; 36(14): 856-62